Constituído pelos rins, ureteres, bexiga e uretra.
A sua formação envolve três tipos de rins:
Pronefro (Figuras 1 e 2): no início da 4ª semana surge um grupo de sete a dez células na região cervical, que formam unidades excretoras, denominadas nefrótomos, rudimentares e não funcionais, que logo se degeneram.
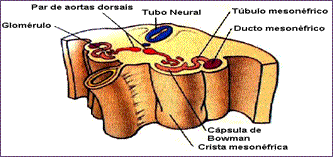
Mesonefro (Figuras 1 e 2): encontra-se na região torácica e lombar superior; surge no fim da 4ª semana; caudal ao pronefro; consiste em glomérulos e túbulos mesonéfricos que se abrem nos ductos mesonéfricos (ou de Wolff) (Figura 4); funcional em um período entre 6 e 10 semanas; degenera no fim do 1º trimestre. No sexo feminino, o mesonefro regride totalmente, enquanto no feto masculino, dá origem ao epidídimo e ducto deferente.
Metanefro (Figura 2): se localiza na região sacral; surge no início da 4ª semana; torna-se funcionante quatro semanas depois; primórdio dos rins permanentes; se desenvolve a partir:
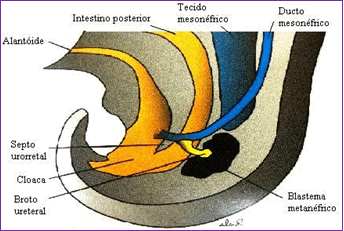
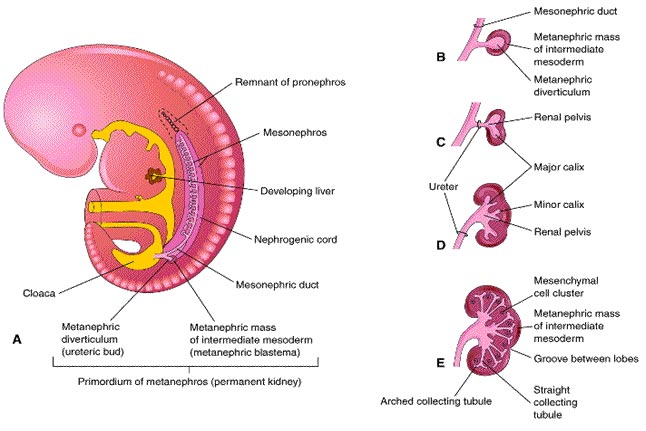
Divertículo Metanéfrico (Broto Ureteral) (Figura 3 e 5):
evaginação do ducto mesonéfrico (de Wolff), próximo à cloaca; primórdio dos ureteres, pelves renais, cálices e túbulos coletores (Figura 6).
Massa Metanéfrica de Mesoderma Intermediário (Blastema Metanefrogênico) (Figura 4): derivado da parte caudal do cordão nefrogênico; origina os glomérulos, cápsula de Bowman, túbulo contorcido distal e proximal e alça de Henle (Figura 6).
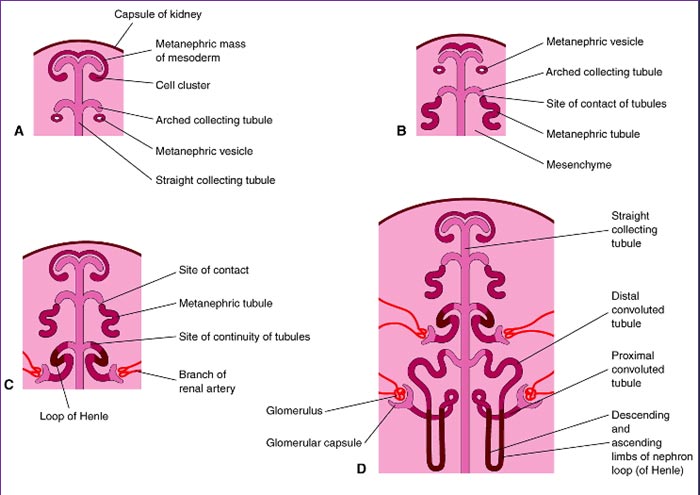
A extremidade do divertículo metanéfrico se dilata, formando a pelve renal primitiva e se divide aproximadamente 15 vezes, formando os futuros cálices maiores e menores. A extremidade dilatada das últimas gerações se denominam ampola. Esta induz o mesênquima adjacente (massa metanéfrica de mesoderma intermediário) a formar uma vesícula (futuros túbulos secretores), que se liga à ampola (futuros túbulos coletores), por volta da 10ª semana. A vesícula assume a forma de “S” e se diferencia em um túbulo coletor e uma cápsula glomerular. O alongamento do túbulo coletor forma o túbulo contorcido proximal, alça de Henle e túbulo contorcido distal. A cápsula e o glomérulo formam o corpúsculo renal. O túbulo coletor e o glomérulo constituem um néfron. Cada glomérulo recebe uma arteríola aferente, que se ramifica e forma um emaranhado capilar dentro da cápsula glomerular. A arteríola eferente, que deixa o glomérulo, se ramifica em torno do túbulo, dando origem as veias coletoras que desembocam no sistema cardinal (Figura 6).
A filtração glomerular começa em torno da 9ª semana fetal, mas a maturação funcional e o aumento da taxa de filtração ocorrem somente após o nascimento.
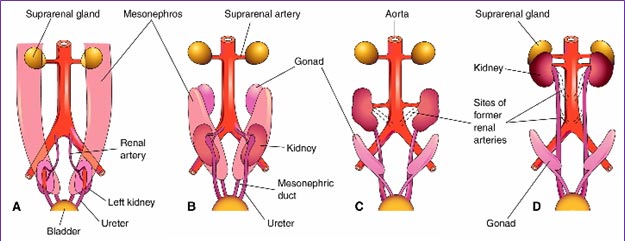
No início, os rins estão na pelve, porém com o crescimento da pelve e do abdome do embrião, os rins se localizam no abdome, chegando à posição adulta na 9ª semana, quando se encontram com as glândulas supra-renais. Assim, as artérias renais que eram ramos das artérias ilíacas comuns, passam progressivamente a ser ramo da extremidade distal da aorta e em seguida da extremidade proximal da aorta. Normalmente, os ramos caudais sofrem involução e desaparecem (Figura 7).
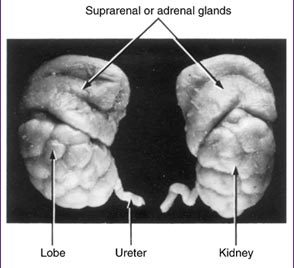
Os rins do feto são lobulados (Figura 8), sendo que esta lobulação tende a desaparecer na infância por causa do aumento e crescimento dos néfrons.
Anomalias
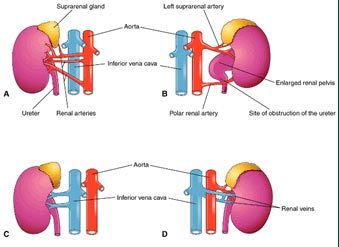
Artérias renais acessórias (supranumerários) (Figura 9): devido a não regressão de uma ou mais artérias renais inferiores transitórias; geralmente a partir da aorta, acima ou abaixo da artéria renal principal; 25% dos rins adultos têm 2 a 4 artérias renais.
Figura 9 – Esquema ilustrativo das variações dos vasos renais supranumerários |
|
Fonte: Moore & Persaud (2003). |
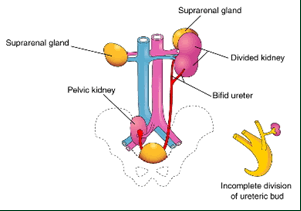
Rins ectópicos (Figura 10): posição anormal, a maioria está localizada na pelve; resultam da não ascensão relativa dos rins.
Figura 10 – Esquema ilustrativo do rim direito pélvico |
|
Fonte: Moore & Persaud (2008). |
|
Bibliografia Consultada:
Moore KL, Persaud TVN. Embriologia clínica. 8a ed. Rio de Janeiro (RJ): Elsevier; 2008.
Moore KL, Persaud TVN. The developing human: clinically oriented embryology. 7th ed. Philadelphia: WB Saunders; 2003.
Schoenwolf GC, Bleyl SB, Brauer PR, Francis-West PH. Larsen embriologia humana. 4a ed. Rio de Janeiro (RJ): Elsevier; 2009.
O’Rahilly R, Müller F. Embriologia & teratologia humanas. 3a ed. Rio de Janeiro (RJ): Guanabara Koogan; 2005.
Sadler TW. Langman embriologia médica. 9a ed. Rio de Janeiro (RJ): Guanabara Koogan; 2005.
1) Sistema Urinário
2) Formação da Bexiga Urinária
|
|
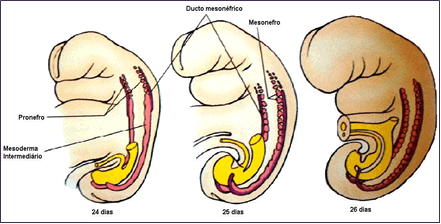
Figura 1 – Esquema ilustrativo do desenvolvimento do pronefro e mesonefro em embriões de 24, 25 e 26 dias
|
 |
|
|
Fonte: Schoenwolf (2009)
|
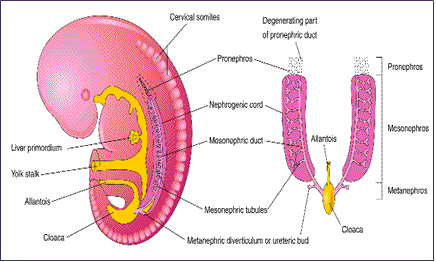
Figura 2 – Esquema ilustrativo do pronefro, mesonefro e metanefro durante a 5ª semana
|
 |
|
|
Fonte: Moore & Persaud (2003)
|
Figura 3 – Esquema ilustrativo do broto ureteral e do blastema metanéfrico
|
 |
|
|
Fonte: Sadler (2005)
|
Correlação clínica
A urina fetal é uma importante fonte de líquido amniótico, principalmente na segunda metade da gravidez. Por isso, situações que interferem na produção de urina ou impedem sua eliminação na cavidade amniótica causam oligoidrâmnio. O feto deglute o líquido amniótico, o que ajuda no desenvolvimento dos pulmões. Ex.: agenesia do rim bilateral ocorre quando os divertículos metanéfricos não se desenvolvem ou os primórdios dos ureteres se degeneram. Leva a hipoplasia pulmonar, devido ao oligoidrâmnio. Essa condição é incompatível com a vida pós-natal.
OBS.: A agenesia renal unilateral geralmente é assintomática.
|
Figura 4 – Esquema ilustrativo do túbulo e ducto mesonéfrico, glomérulo e cápsula de Bowman
|
 |
|
|
Fonte: Schoenwolf (2009)
|
Figura 5 – Esquema ilustrativo do desenvolvimento do rim permanente
|
 |
|
|
Fonte: Moore & Persaud (2003)
|
Figura 6 – Esquema ilustrativo do desenvolvimento dos néfrons
|
 |
|
|
Fonte: Moore & Persaud (2003)
|
Figura 7 – Esquema ilustrativo da ascensão dos rins e modificação das artérias renais
|
 |
|
|
Fonte: Moore & Persaud (2003)
|
Figura 8 – Esquema ilustrativo dos lobos renais
|
 |
|
|
Fonte: Moore & Persaud (2003)
|
|
